| 固体の溶解度 |
| 溶媒100gに最大限溶けることのできる(無水物としての)溶質の質量[g] |
【例題】硫酸銅(II) CuSO4の水に対する溶解度は、25
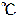 で22.2、80
で22.2、80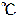 で56.0である。
で56.0である。
80
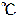 の硫酸銅(II) 飽和水溶液100gを25
の硫酸銅(II) 飽和水溶液100gを25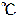 に冷却したとき、析出する結晶がすべて硫酸銅(II) 5水和物 CuSO4・5H2O だったとすると、その質量はいくらか?
に冷却したとき、析出する結晶がすべて硫酸銅(II) 5水和物 CuSO4・5H2O だったとすると、その質量はいくらか?
析出する硫酸銅(II)5水和物CuSO4・5H2Oの質量をx [g]とすると、
式量は、CuSO4 = 160 , CuSO4・5H2O = 250 であるから、xのうち、160/250が溶質から、90/250が溶媒から、それぞれ失われたことになる。
| 溶質 | 溶媒 | 溶液 | |
| 80℃ | 100 | ||
| 56.0 | 100 | 156.0 | |
| 25℃ | 100-x | ||
| 22.2 | 100 | 122.2 |
こうして得られた、析出後の溶質と溶媒の質量の比は、25℃における飽和水溶液の溶質、溶媒比に等しいから、
これを解いて、