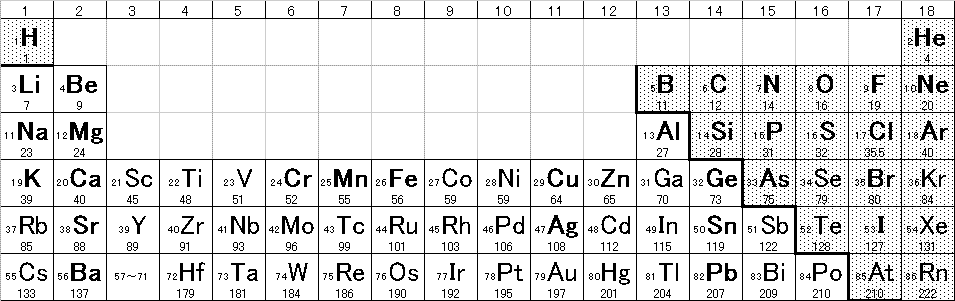
- 金属元素/非金属元素
- 第1イオン化エネルギー/電子親和力/電気陰性度
- 金属結合/イオン結合/共有結合

- この世で一番「酸化力」の強い物質は?、では、二番目は?
- 「金属のイオン化傾向」とは、何の順位?
- 分子の「極性」。沸点の高低、親水性/疎水性。「水」という物質の異常な性質。
- 「生物」を構成する基本元素は?、そして、「無生物」を構成する基本元素は?
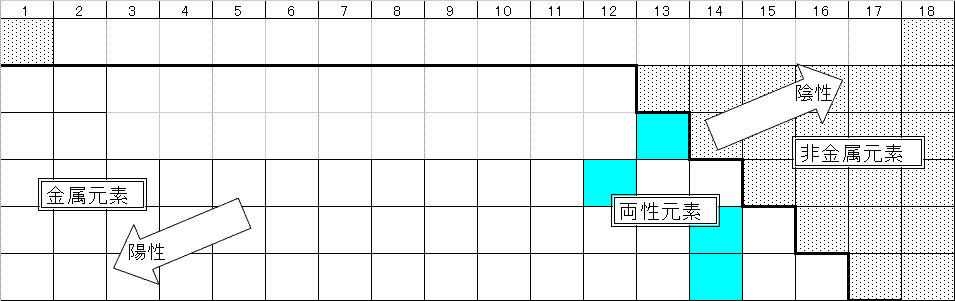
- 「オクテット則」と、分子の立体構造。この世で一番「硬い」物質は?
- 下の図を用いて、メタン、アンモニア、水、塩化水素、の立体構造を描け。



(3)[ハロゲン](2004追4-4)
(1)[ハロゲン](2007追3-4)
- 酸化数を決めるのに、水素Hを+1、酸素を-2として計算せよ、というのは、何故なのだろう?
本当の、酸化数の決め方。エタノールの二つの炭素の酸化数は?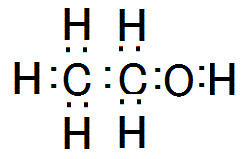
- フェノールC6H5-OHは、酸、
エタノールCH3-CH2-OHは、中性、
水酸化ナトリウムNaOHは塩基、
いったい「-OH」という構造はなんなのだ?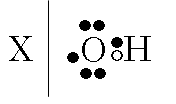
金属水酸化物は、塩基性水酸化物である。非金属の水酸化物とは、つまり、オキソ酸のことである。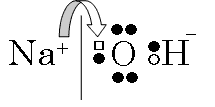
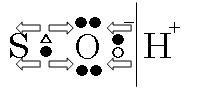
- 電離度


「電離度」は、濃度が小さくなると、大きくなる!
どんな弱酸でも、薄めれば、かならず、電離度は1に近づく。
- 電離平衡定数
たとえば、弱酸である酢酸について。
酢酸の初期濃度を c mol/L 、電離度を α とする。溶液1Lについて、
電離平衡定数 Ka は、CH3COOH H+ + CH3COO- はじめ c 電離 cα cα cα 平衡後 c(1-α) cα cα
Ka= [H+][CH3COO-] = (cα)(cα) = cα2 [CH3COOH] c(1-α) 1-α - この式は、αについての2次方程式
cα2 + Kaα - Ka = 0
であり、これを解けば、
・・・(i)
と、電離度を計算することができるが、
- ここで、αが充分に1より小さい場合、1-α
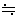 1 として
1 として
・・・(ii)
という近似式を用いることができる。
- この式は、αについての2次方程式

