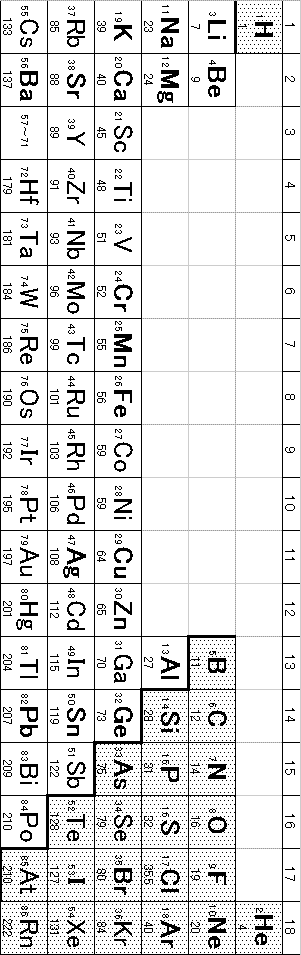
- 「非金属」-「非金属」間は共有結合、「金属」-「非金属」間はイオン結合、「金属」-「金属」間は金属結合、
- (1)炭素(C)の共有結合による、共有結合結晶
- (2)水(H2O)分子の分子間力による、分子結晶
- (3)二酸化炭素(CO2)分子の分子間力による、分子結晶
- (4)サリチル酸(C6H4(OH)COOH)分子の分子間力による、分子結晶
- (5)イオン対(NaCl)の静電引力による、イオン結晶
- (6)金属(Pt)の、金属結晶
| CO2 | CH4 | NH3 |
| O=C=O 「直線」 | 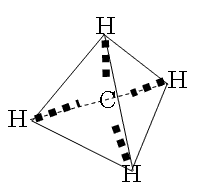 「正四面体」 | 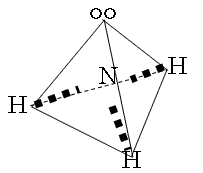 「正三角錐」 |
| CH2=CH2 | C2H2 | H2O |
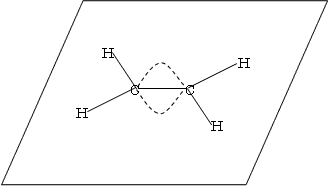 「平面」 | 「直線」 | 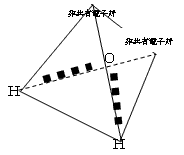 「折れ線」 |
- 物質量(モル数)を合わせる
2NO2→N2 - 酸化数の変化を調べる
2NO2(+4)→N2(0) - 酸化数の変化に見合った電子の移動を考える
2NO2(+4)+8e-→N2(0) - 両辺の電荷をそろえる(H+またはOH-を加える)
「左辺」に加えるには、「反応前」の液性(酸か塩基か?)を考えなければならない。ここでは酸性だった、としている。二酸化窒素は酸性酸化物だし!
2NO2(+4)+8e-+8H+→N2(0) - 両辺の物質量をそろえる(H2Oを加える)
「質量保存則」だ!
2NO2(+4)+8e-+8H+→N2(0)+4H2O
- 4He 「質量数」4。「質量数」=「陽子数」+「中性子数」
- 2He 「原子番号」2。「原子番号」=「陽子数」
- He+ 1価の陽イオン。「電子数」=「原子番号」=「陽子数」、だったはずだ。しかし電子を一個失ったから1価の陽イオンになった。
| 陽子 | 中性子 | 電子 |
| 2 | 2 | 1 |
- 2NaN3+CuO→3N2+Na2O+Cu
化学反応式上の物質量の比 NaN3 CuO N2 2 1 3 - すべての気体は標準状態で1molあたり、22.4Lだから、
実際に発生した「気体」すなわち窒素N2は、44.8[L]÷22.4[L/mol]=2[mol] - 「式量」=「モル質量」は、アジ化ナトリウムNaN3=23+14×3=65、酸化銅(II)CuO=64+16=80、
必要なアジ化ナトリウムNaN3の質量x[g]、酸化銅(II)CuOの質量y[g]、とすると、実際に起こった反応での物質量の比 NaN3 CuO N2 x 
65 y 
80 44.8 
22.4 - これらを「比」の式としてつないで、
すなわち、x 
65 : y 
80 : 2 = 2:1:3 x 
65 : 2 = 2:3 y 
80 : 2 = 1:3 x+y= 2×2×65 
3 + 2×1×80 
3 = 140
- エチレン(CH2=CH2)1分子をつくるには、炭素原子(C)が2個必要だ。
- 自然界の炭素は、99%の普通の12Cと、1%の13Cとでできている。
ということは、たくさんの炭素原子のつまった「袋」の中から、1個の炭素原子を「選び出す」ときに、それが- 13Cである「確率」pが、p=0.01
- 12Cである「確率」1-pが、1-p=0.99 である、と言ってよい。
- さて、無数の炭素原子のはいった「袋」から、たった2個の炭素原子を「取り出し」て、エチレンを組み立てるとき、出来上がったエチレンが、
- 13CH2=13CH2である確率は、p2
- 12CH2=13CH2である確率は、12CH2=13CH2である場合と13CH2=12CH2である場合を考慮して(!)、2!×p(1-p)
- 12CH2=12CH2である確率は、(1-p)2
- これはちゃんと、「二項定理」、
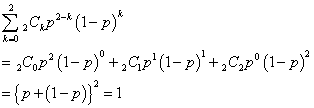
の各項を表しておりますでしょ? - したがって、出来上がりの1mol、すなわちアボガドロ数NA=6.02×1023個のエチレン分子の内訳は、
- 13CH2=13CH2は、p2NA=0.012×6.02×1023=10-4×6.02×1023=6.02×1019
- 12CH2=13CH2は、2p(1-p)NA=2×0.01×0.99×6.02×1023=1.98×10-2×6.02×1023
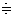 2×6.02×1021
2×6.02×1021
- 12CH2=12CH2は、(1-p)2NA=0.992×6.02×1023
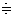 6.02×1023
6.02×1023
- (2)
- 気体は、その種類にかかわらず、標準状態で22.4Lの体積を占めることが知られているから、その「密度(比重)」、すなわち「質量÷体積」の大小は、
「モル質量=分子量」を比較するだけで、わかる。 - 空気は、窒素N2=14×2=28、酸素O2=16×2=32が、約4:1の割合でできた混合気体と考えられるから、その「平均分子量」は、
28×4+32×1 
1+4 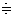
29 - ある気体が、空気より軽くて「浮く」のか?、重くて「沈む」のか?、を判断するには、その気体の「分子量」と29を比較すればよいことになる。
メタンCH4=12+4=16は、29よりはるかに小さく、「浮く」、つまり「上方に滞留する」ことになる。
- 気体は、その種類にかかわらず、標準状態で22.4Lの体積を占めることが知られているから、その「密度(比重)」、すなわち「質量÷体積」の大小は、
- Q=53-227+1299+286=1411
C2H4(気) + 3O2(気) = 2CO2(気) + 2H2O(液) + Q[kJ] ・・・ エチレンの燃焼熱 ------ ------ ------ ------ ------ C2H4(気) = 2C(黒鉛) + 2H2(気) + 53[kJ] ・・・ エチレンの生成熱 2C(黒鉛) + H2(気) = C2H2(気) - 227[kJ] ・・・ アセチレンの生成熱 C2H2(気) + 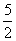 O2(気)
O2(気)= 2CO2(気) + H2O(液) + 1299[kJ] ・・・ アセチレンの燃焼熱 H2(気) + 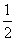 O2(気)
O2(気)= H2O(液) + 286[kJ] ・・・ 水の生成熱

Q1+39=Q2+44
Q2=Q1-5
- (1)有機酸の強さ、カルボン酸>二酸化炭素>フェノール
- (2)リン酸H3PO4
- (3)酸が「強い」とは、電離度が高い、同じ物質量あたりで比較すると、発生する水素イオンの量が多い、ということである。発生する水素イオンの量が多ければ、これが亜鉛表面で「還元」されて、発生する水素分子の量も多いだろう。
- (4)
- pHは、水素イオン濃度[mol/L]の常用対数にマイナスをつけたもの、である。
pH=-log10[H+] - 水素イオン濃度[H+]と水酸化物イオン濃度[OH-]の積は一定である(水のイオン積)。
[H+]×[OH-]=10-14 - だから、
pH=-log10[H+]=14+log10[OH-] - つまり、
- 底が1より大きい対数関数は、単調増加関数であること、
- [H+]も[OH-]も、1よりはるかに小さい数であること、
- 酸を10倍に薄めるごとに、pHは1ずつ増えて、だんだん中性pH=7に近づく。
- 塩基を10倍に薄めるごとに、pHは1ずつ減って、だんだん中性pH=7に近づく。
- pHは、水素イオン濃度[mol/L]の常用対数にマイナスをつけたもの、である。
- 濃度c[mol/L]の弱酸HAの溶液1[L]があったとしよう。もちろん、すでに、電離している、のだが、
まだ電離していない、状態を想定すると、そこにはc[mol]のHAがあったはずだ。 - 電離度をαとすると(αはもちろん0と1の間の数である)、電離後の状態は、以下の表のようになり、
HA → H+ + A- はじめ c - - 電離 cα cα cα ____ ____ ____ ____ 電離後 c(1-α) cα cα - 1[L]の溶液中に、水素イオンH+が、cα[mol]存在していることになる。つまり、水素イオン濃度[H+]は、
[H+]=cα - c=0.10[mol/L]、α=2.0×10-2であるから、
[H+]=0.10×2.0×10-2=2.0×10-3 - ここで、pH=-log10[H+]なのだが、別に対数の計算をしなくとも、
1.0×10-3<2.0×10-3<10.0×10-3=1.0×10-2
1.0×10-3<[H+]<1.0×10-2
であることくらいは、わかる。つまり、pHは、2と3の間、である。
- (1)塩素酸カリウムから酸素が発生する、といっているから、それは、オキソ酸に含まれていた化合物中の酸素(かならず「-2価」)が、単体「0価」の酸素になったのだから、その酸化還元反応式を作ってみよう。
- 酸化剤は「誰」か?
塩素の最外殻電子は7個、だから、最高の酸化数は+7、最低の酸化数は-1である。
塩素酸は、+5というかなり高い酸化数をもっている。これが塩化物イオンCl-、酸化数-1まで還元されることによって、「酸化剤」の能力を発揮するのだろう。化合物 酸化数 塩化水素(塩酸)HCl -1 塩素Cl2 0 次亜塩素酸HClO +1 亜塩素酸HClO2 +3 塩素酸HClO3 +5 過塩素酸HClO4 +7 - 酸化数の変化を調べる
ClO3-(+5)→Cl-(-1) - 酸化数の変化に見合った電子の移動を考える
ClO3-(+5)+6e-→Cl-(-1) - 両辺の電荷をそろえる(H+またはOH-を加える)
ClO3-(+5)+6e-+6H+→Cl-(-1) - 両辺の物質量をそろえる(H2Oを加える)
ClO3-(+5)+6e-+6H+→Cl-(-1)+3H2O・・・(ア)
- 酸化数の変化を調べる
- 還元剤は「誰」か?
酸素が発生した、というのだから、どこにでもある酸素化合物として水H2O、にしておこう。- 物質量をそろえる
2H2O→O2 - 酸化数の変化を調べる
2H2O(-2)→O2(0) - 酸化数の変化に見合った電子の移動を考える
2H2O(-2)→O2(0)+4e- - 両辺の電荷をそろえる(H+またはOH-を加える)
2H2O(-2)→O2(0)+4e-+4H+・・・(イ) - 両辺の物質量は、そろっている(!)
- 物質量をそろえる
- 全反応式を作る。
(ア)(イ)から、電子が過不足なくやり取りできるように、(ア)を2倍、(イ)を3倍して辺々加える。
という結果になった。2ClO3-+12e-+12H+ → 2Cl-+6H2O ・・・(ア)×2 6H2O → 3O2+12e-+12H+ ・・・(イ)×3 2ClO3- → 2Cl-+3O2 - 酸化マンガン(IV)は、酸化還元反応自体には、何の役割も果たしていない。つまり、「触媒」である。
であるから、酸化マンガン(IV)も酸化剤として働く場合もあるが、ここではもっと強力な塩素酸イオンが、酸化剤だったのだから、出番はなかった。化合物 酸化数 マンガン金属単体Mn 0 マンガンイオン(II)Mn+2 +2 酸化マンガン(IV)MnO2 +4 過マンガン酸カリウムKMNO4 +7
- 酸化剤は「誰」か?
- イオン化傾向が水素(H2)より大きい金属は、
- 金属単体が「還元剤」として、
Ca→Ca2++2e- - 水、または、希酸に含まれる水素イオン(H+)を「酸化剤」として、
2H2O+2e-→H2+2OH-
2H++2e-→H2
- 金属単体が「還元剤」として、
- 常温の水と、すなわち熱エネルギーを加えられなくても反応するのは、その中でも、特にイオン化傾向が高い金属である。
(ア)から、A>C、(イ)から、A>B - C++B→C+B+
- Cの陽イオンC+が「還元」されCの単体Cになり、
- Bの単体Bが「酸化」されBの陽イオンB+になった。
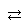 H++HS-
H++HS-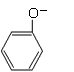 ・・・(エ)
・・・(エ)
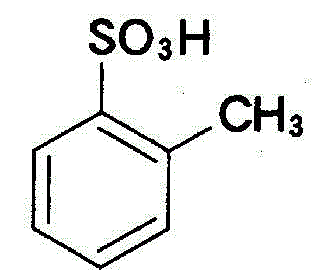 +NaOH→
+NaOH→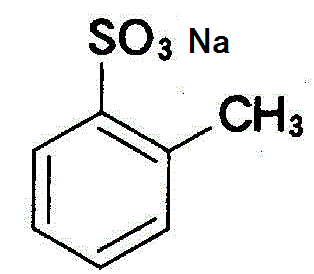 +H2O
+H2O
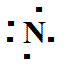
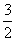 H2O
H2O
 :2分子から脱水して、ジエチルエーテル
:2分子から脱水して、ジエチルエーテル
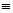 CH
CH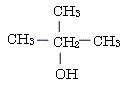 :(第3級アルコール)
:(第3級アルコール)